
斯璐教授
《CSCO免疫检查点抑制剂相关毒性管理指南》执笔人《Clinical Cancer Research》审稿专家
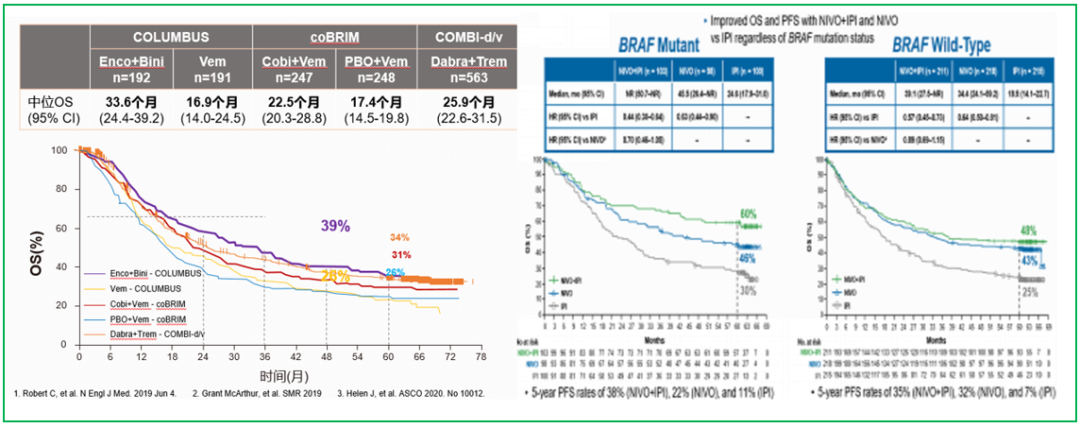
对于晚期黑色素瘤的BRAF-V600突变患者来说,双靶(3项研究结果:Columbus,CoBRIM,COMBI-D/V,左下图)和双免(CM067研究,右下图)都有较高的有效率和长期生存率。因此,对于一线该先使用双免还是双靶?业界一直在争论。
去年ESMO会议报道的CheckMate-067研究5年生存随访数据显示,BRAF突变患者使用双免优于野生型患者;而今年ASCO会议的一项真实世界回顾分析又显示,BRAF野生型患者使用双免的生存获益优于BRAF突变型患者。这些结论让双免和双靶之争进入了白热化阶段。
本次ESMO会议带来的SECOMBIT研究在一定程度上对这一问题进行了解答。
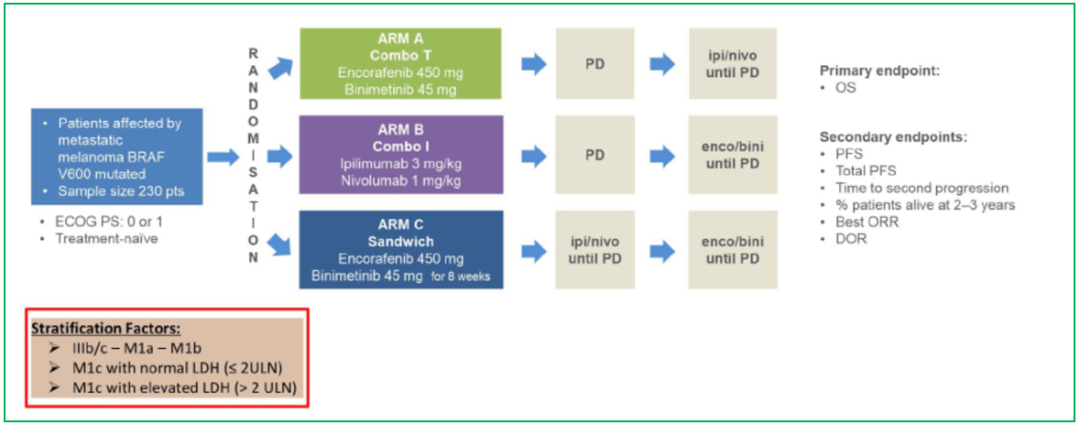
SECOMBIT研究是一项Ⅱ期临床研究,2015年开始设计,分成3组:A组先双靶(E+B),PD后换用双免(N1+I3);B组先双免(N1+I3),PD后换用双靶(E+B);C组相当于在B组前加了8周E+B诱导期,简称三明治组。每组预计入组约70例患者。主要研究终点为OS,中位随访时间17个月。
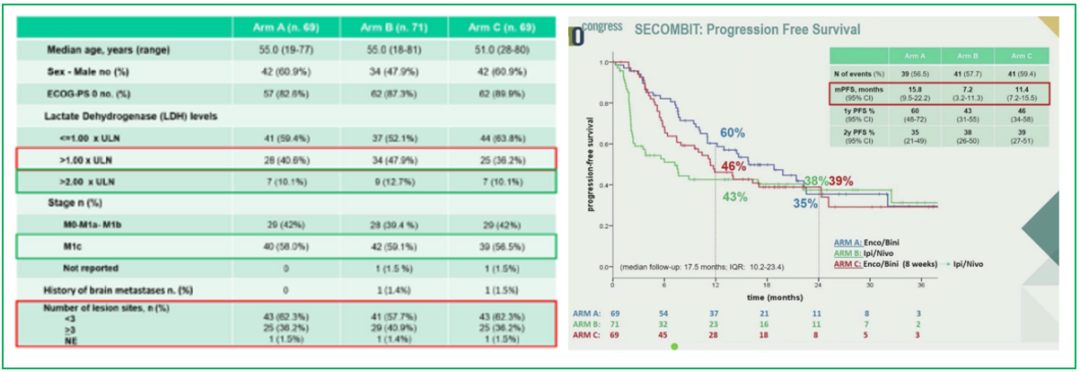
从一般特征看,B组LDH正常患者最少,<3个转移灶的比例最少(左下图)。从生存结果看(右下图),三组的PFS分别为15.8m、7.2m和11.4m,1年的PFS率为60%,43%和46%,2年的PFS率分别为35%、38%和39%。
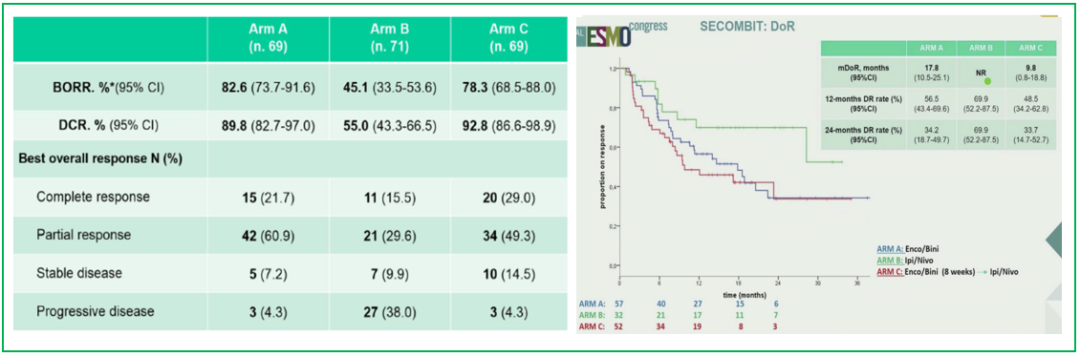
从疗效分析看,三组的有效率(左下图)分别为82.6%、45.1%和78.3%,C组的CR率最高(29%),从疗效维持时间看(右下图),B组的1年和2年的疗效维持患者的比例更高,中位DOR未达到。
从毒副反应看,A组和C组明显小于B组。
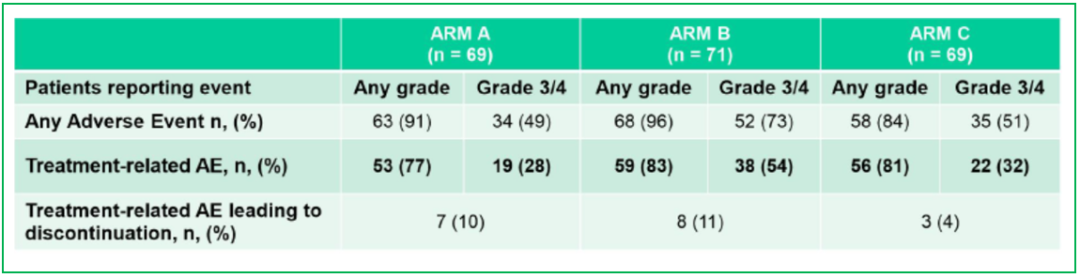
1、双靶先上场似乎更好?本次会议公布的仍是早期结果,从CR率和2年PFS率来看,似乎C组有胜出趋势;但A组的PFS最长,有效率也最高;B组虽爆发力不足,但属于耐力型选手,在2年PFS率上,追平其他两组。但不管如何,A和C组存在更多的优势,而这两组均是双靶先上场。
2、毒副反应看?该研究于2015年开始设计,那时候双免的标准剂量是N1I3,疗效高但毒性也大,在该研究中这一特点表现得淋漓尽致;而我们目前临床实践中一般使用N3I1,甚至Ipi剂量更低,是否能重复出2年PFS这样的结果,很难预计。
3、序贯还是联合?从KN022、IMspire 150和COMBI-i三项靶免联合(单免)的研究看,中位PFS也为15~16m,与A组序贯治疗的PFS相仿。从经济学和副反应来看,似乎靶免(单免)联合比序贯要更胜一筹!当然还期待一项Ⅲ期随机对照临床研究——DREAMseq研究(分两组先双免(NI3或N3I1)后双靶,或者先双靶后双免(NI3或N3I1));和两项Ⅱ期临床研究——ImmunoCobiVem研究(一组是先V+C,PD后换用阿特珠单抗;另一组正好相反)和EORTC EBIN研究(一组先双免N3I1,PD后研究者自行决定后续治疗;另一组E+B诱导12周后双免N3I1,PD后再使用E+B)。
4、总生存如何?OS为本研究的主要终点,由于随访时间较短,目前暂未报道OS结果,预计2021年下半年报道。从PFS2来看,A组和B组在24个月后基本重合,并进入拖尾期。因此预测A/B两组OS可能趋于一致。
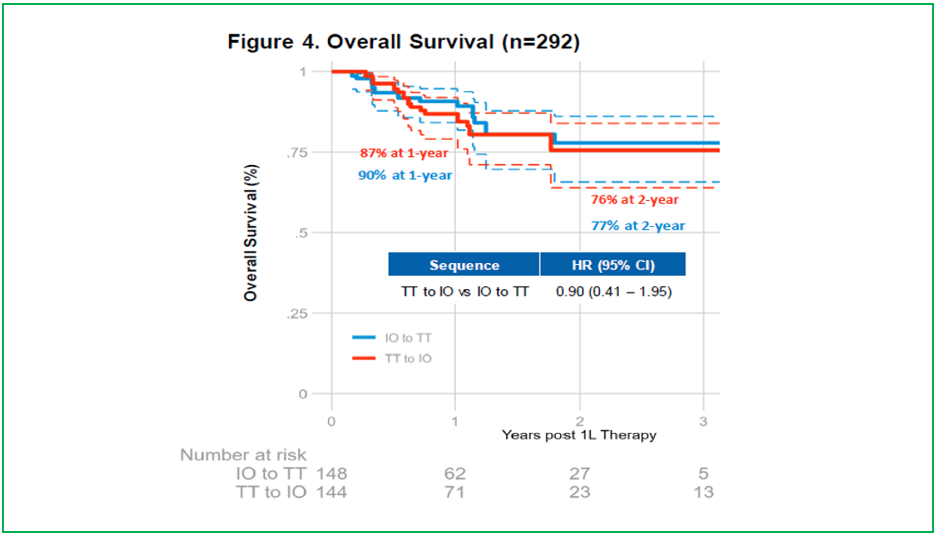
此外,今年ESMO报道了一篇靶向(TT)和免疫(IO)序贯的真实世界数据(摘要号1108P)。该研究收集了296名1L和2L治疗(IO和TT)的BRAF+晚期黑色素瘤患者数据。结果显示两组OS曲线基本重合,TT-IO患者的2年OS为76%,而IO-TT为77%。没有统计学差异。
BRAF-V600突变的话题,先免疫还是先靶向?联合还是序贯?到目前为止还是没有明确答案。总体而言,在我国临床实践中,BRAFi±MEKi仍然是快速减瘤的主要手段,也是不可否认的标准治疗。?