编者按:对于乳腺癌患者来说,人类表皮生长因子受体HER2靶向治疗的临床应用,改变了HER2阳性乳腺癌的治疗模式,改善了患者的预后。靶向药物在乳腺癌新辅助治疗、辅助治疗和解救治疗阶段均取得了长足发展,提高了我国HER2阳性乳腺癌的治疗水平。本期我们将介绍一例经新辅助治疗后仍有残余病灶的HER2阳性乳腺癌患者,术后辅助治疗的相关依据。
周女士,2020年3月无意中发现右侧乳房有一肿物,到医院检查后,给予右乳肿物以及腋下肿大淋巴结穿刺活检,病理回报:乳腺浸润性癌,免疫组化回报为:ER(﹣)、PR(﹣)、HER2(3﹢),Ki-67(30%),右腋下淋巴结穿刺为淋巴结转移癌。
医生建议先行化疗,再进行手术。于是,周女士接受了TCbHP 6次化疗,后给予手术治疗,术后病理回报为:乳腺浸润性癌。浸润性癌镜下最大灶0.5 cm,MP分级3级,淋巴结未见转移0/15,周女士听说她需要一个伴有“生物导弹”的靶向药物治疗1年,且花费较大。对此,周女士心生困惑,为解决患者的疑虑,医生向患者介绍了KATHERINE研究的相关背景及研究数据结果,以安慰患者。
研究背景:HER2阳性早期乳腺癌新辅助化疗联合抗HER2靶向治疗后有残存浸润性病灶的患者,其疾病复发和死亡风险更高。KATHERINE研究旨在评价以T-DM1替代曲妥珠单抗作为新辅助治疗后有残存病灶患者的辅助治疗方案。
研究设计:研究入组患者为cT1-4/N0-3/M0、经新辅助治疗后仍然有残留病灶的HER2阳性乳腺癌患者,新辅助化疗要求至少6个周期(不少于9w的紫杉醇,允许使用蒽环和烷化剂,化疗均在术前完成),新辅助靶向治疗要求至少曲妥珠单抗9w(允许双靶)。患者术后12w随机分配至T-DM1组(3.6 mg/kg IV Q3W,共14周期)和曲妥珠单抗组(6 mg/kg IV Q3W,共14周期),主要终点为iDFS(预设的最终目标为3年iDFS率从曲妥珠单抗组的70.0%提高至T-DM1组的76.5%,HR 0.75)。研究于2013年4月3日至2015年12月31日共入组了1486例患者(曲妥珠单抗组和T-DM1各743例)。
入组基线情况及ITT人群分层情况见下表。
研究结果:2018年SABCS大会上报道了中位随访41个月的初次分析显示,相较于曲妥珠单抗组,T-DM1组患者的3年DFS率显著提高了11.3%(77.0% vs 88.3%,HR0.50,95% CI:0.39~0.64),乳腺癌侵袭性复发风险或死亡的降低了50%。
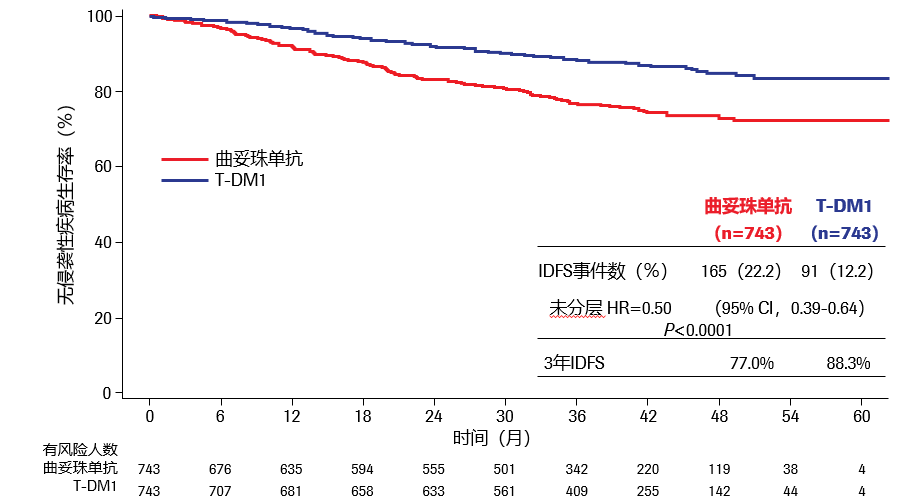
亚组分析可见,无论患者何种分期、HR表达状态、术前双靶或单靶、术后腋结状态均可从T-DM1辅助治疗中获益。对于新辅助治疗后腋结阴性、残存病灶≤1cm等肿瘤负荷较低的患者(ypT1a,ypT1b或ypT1mic 和ypN0),也能够从T-DM1治疗中获益(HR 0.60,95%CI:0.33~1.12);此外,KATHERINE研究中有77例临床分期为T1cN0(T-DM1组45例),其中曲妥珠单抗组有6例患者发生iDFS事件,3年iDFS率为81%(26/32),而T-DM1组尚未发生iDFS事件。
对于RCB评分较好或残余病灶较小的患者,我们看到在KATHERINE研究中仍然有获益,我们仍然推荐这部分患者使用T-DM1治疗。
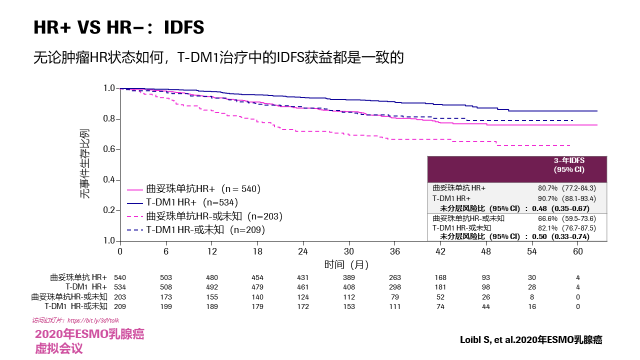
T-DM1的治疗作用并不依赖于HER2状态:
在今年的ESMO-Breast cancer会议上,我们报道了这样一个结果,对KATHERINE研究中新辅助治疗后non-pCR患者的手术标本重新进行免疫组化检查发现,在70例残留病灶HER2检测阴性的患者中,42例随机分配接受曲妥珠单抗治疗的患者发生了11例iDFS事件,28例随机分配接受T-DM1治疗的患者发生了0例IDFS事件,这再次证明了这些患者是可以从T-DM1的研究中获益的,与我们之前的试验结果是一致的,这对于临床是很有意义的结果。
生物标志物表达水平与抗HER2靶向治疗结局的关系:
我们又对新辅助治疗前和/或手术标本进行了进一步的基因表达分析,并在ASCO大会上公布了结果,研究发现,PIK3CA突变状态并不影响曲妥珠单抗或T-DM1的治疗结局,T-DM1在HER2低表达组和高表达组的获益一致,此外,PD-L1、CD8、Teff等所有参与评估的生物标志物水平均不影响T-DM1的治疗获益。
耐受性方面:
在安全性方面,总体上来说,大部分患者还是耐受的。对于因AE而停止治疗的患者,我们对于停药标准的把控是非常严格的,对于实验室指标异常的患者我们进行了停药,导致没能完成最终的治疗,但这部分患者并未出现真正的临床症状;对于血小板降低的患者,我们也是能够进行很好的管理的,所以这个药物的耐受性总体上是良好的,对于考虑使用T-DM1的患者,不应该受到这样一些AE的顾虑和影响。

T-DM1联合放疗:
可以看到T-DM1的使用不受放疗影响,也没有证据证明两者联合会增加肺部毒性。
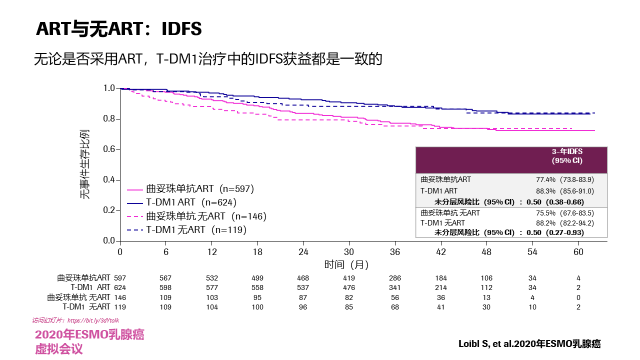
T-DM1联合内分泌治疗:
在接受和未接受内分泌治疗中,两组的HR是无差异的。
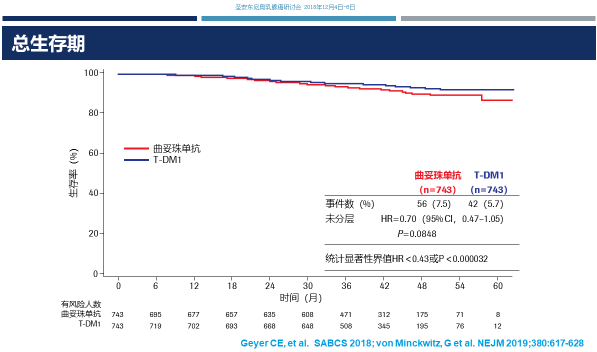
总生存:曲妥珠单抗组vs T-DM1组的事件数是56 vs 42,未分层风险比是0.7,当然我们还需要进一步随访,等待OS的成熟。
指南推荐情况:KATHERINE研究结果无疑对HER2+早期乳腺癌标准治疗管理产生了很大的影响,T-DM1给患者带来了获益也改变了临床实践,同时也受到了全球多个指南推荐。
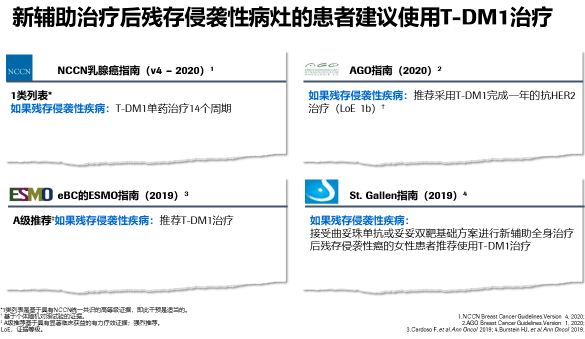
最后医生解释道,从此研究结果来看,新辅助接受双靶治疗non-pCR的患者,后经接受T-DM1的治疗组获益更加明显:高出4%,所以针对这部分的患者需要使用T-DM1治疗。而且T-DM1也没有对患者的生活质量产生特别不好的影响,所以,我认为还是需要去尝试T-DM1的治疗。
 ?
?
武汉大学医学博士,硕士研究生导师
内蒙古肿瘤医院博士团人才
中国乳腺微创与乳腔镜手术联盟常务理事
中国医药教育协会乳腺疾病青年委员会委员
北京乳腺病防治学会国际医疗与合作专委会委员
北京肿瘤防治研究会乳腺癌分会委北京员
北京癌症防治学会精准靶向专委会委员
内蒙古乳腺疾病防治学会副理事长兼副秘书长
内蒙古中西医结合乳腺病防治学会秘书长
内蒙古抗癌学会乳腺青年专业委员会常委
内蒙古肿瘤防治学会专业委员会委员
农工党自治区医疗工作委员会委员





 京公网安备 11010502033352号
京公网安备 11010502033352号